KB 4 PERKEMBANGAN TEORI ATOM
Perkembangan Teori Atom: Model Dalton, Thomson, Rutherford, dan Bohr
Pada beberapa abad sebelum masehi, filsuf-filsuf Yunani, di antaranya Leucippus dan Democritus berpendapat bahwa semua materi terdiri dari partikel-partikel kecil yang tak terbagi. Democritus menyatakan bahwa jika suatu materi dibagi menjadi bagian yang lebih kecil kemudian terus dibagi lagi maka akan sampai pada suatu saat di mana didapat bagian yang sangat kecil yang tidak dapat dihancurkan atau dibagi lagi yang disebut atom (‘atomos’ dalam bahasa Yunani yang artinya ‘tak terbagi’).
Namun, pemikiran filosofis tersebut tidak begitu diterima pada saat itu hingga pada awal abad ke-18, John Dalton merumuskan teori atom yang berhasil menjelaskan hukum-hukum dasar kimia – hukum kekekalan massa, hukum perbandingan tetap, dan hukum kelipatan perbandingan.
Teori Atom Dalton
Teori
atom Dalton menyatakan bahwa:
1. Setiap unsur tersusun dari partikel yang sangat teramat kecil yang
disebut atom.
2. Semua atom dari satu unsur yang sama adalah identik, namun atom
unsur satu berbeda dengan atom unsur-unsur lainnya.
3.
Atom dari satu unsur
tidak dapat diubah menjadi atom dari unsur lain melalui reaksi kimia; atom
tidak dapat diciptakan ataupun dimusnahkan dalam reaksi kimia.
4.
Senyawa terbentuk dari
kombinasi atom-atom dari unsur-unsur yang berbeda dengan rasio atom yang
spesifik.
5.
Teori atom Dalton ini
memberikan gambaran model atom seperti model
bola pejal atau model bola billiard.
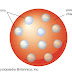
Teori Atom J.J. Thomson
Pada
tahun 1897, J.J. Thomson melakukan eksperimen dengan sinar katoda. Eksperimen
tersebut menunjukkan bahwa sinar katoda terdefleksi (terbelokkan) oleh medan magnet maupun medan listrik. Hal ini menunjukkan
bahwa sinar katoda merupakan radiasi partikel yang bermuatan listrik. Pada
eksperimen dengan medan listrik, sinar katoda terbelokkan menuju ke arah kutub
bermuatan positif. Hal ini menunjukkan bahwa sinar katoda merupakan radiasi
partikel bermuatan negatif. Selanjutnya, partikel sinar katoda ini disebut
sebagai elektron. Penemuan elektron ini kemudian mengacu pada kesimpulan bahwa
di dalam atom terdapat elektron yang bermuatan negatif. Menurut model atom
Thomson, elektron bermuatan negatif tersebar dalam bola bermuatan positif
seperti model roti kismis, di mana kismis-kismis adalah elektron-elektron, dan
roti adalah bola bermuatan positif.
Teori Atom Rutherford
Pada tahun 1911, Ernest Rutherford melakukan eksperimen menembakkan partikel α — partikel bermuatan positif — pada lempeng emas tipis. Ia menemukan bahwa sebagian besar partikel-partikel α tersebut menembus melewati lempeng emas, namun ada sebagian yang mengalami pembelokan bahkan terpantulkan. Hal ini mengacu pada kesimpulan model atom Rutherford: model inti, di mana dalam atom yang sebagian besar merupakan ruang kosong terdapat inti yang padat pejal dan masif bermuatan positif yang disebut sebagai inti atom; dan elektron-elektron bermuatan negatif yang mengitari inti atom.
Teori Atom Bohr
Pada tahun 1913, Niels Bohr mengajukan
model atom untuk menjelaskan fenomena penampakan sinar dari unsur-unsur ketika
dikenakan pada nyala api ataupun tegangan listrik tinggi. Model atom yang ia
ajukan secara khusus merupakan model atom hidrogen untuk menjelaskan fenomena
spektrum garis atom hidrogen. Bohr menyatakan bahwa elektron-elektron bermuatan
negatif bergerak mengelilingi inti atom bermuatan positif pada jarak tertentu
yang berbeda-beda seperti orbit planet-planet mengitari matahari. Oleh karena
itu, model atom Bohr disebut juga model tata surya
Setiap lintasan orbit
elektron berada tingkat energi yang berbeda; semakin jauh lintasan orbit dari
inti, semakin tinggi tingkat energi. Lintasan orbit elektron ini disebut juga
kulit elektron. Ketika elektron jatuh dari orbit yang lebih luar ke orbit yang
lebih dalam, sinar yang diradiasikan bergantung pada tingkat energi dari kedua lintasan
orbit tersebut.
Teori Atom Mekanika
Kuantum
Pada tahun 1924, Louis de Broglie menyatakan
hipotesis dualisme partikel-gelombang — semua materi dapat memiliki sifat
seperti gelombang. Elektron memiliki sifat seperti partikel dan juga sifat
seperti gelombang. Pada tahun 1926, Erwin Schrödinger merumuskan
persamaan matematis yang kini disebut persamaan gelombang Schrödinger, yang
memperhitungkan sifat seperti partikel dan seperti gelombang dari elektron.
Pada tahun 1927, Werner Heisenberg mengajukan asas ketidakpastian Heisenberg
yang menyatakan bahwa posisi elektron tidak dapat ditentukan secara pasti,
namun hanya dapat ditentukan peluang posisinya.
Teori-teori
— dualisme partikel gelombang, asas ketidakpastian Heisenberg, dan persamaan
Schrödinger—ini kemudian menjadi dasar dari teori atom mekanika kuantum.
Penyelesaian persamaan Schrödinger menghasilkan fungsi gelombang yang disebut
orbital. Orbital biasanya digambarkan seperti awan elektron, di mana
kerapatan awan tersebut menunjukkan peluang posisi elektron. Semakin rapat awan
elektron maka semakin tinggi peluang elektron, begitu pula sebaliknya. Oleh
karena itu, model atom mekanika kuantum disebut juga model awan elektron.
Sebelumnya, pada tahun 1919,
Rutherford berhasil menemukan partikel bermuatan positif, yang disebut proton,
dari eksperimen penembakkan partikel α pada atom nitrogen di udara. Lalu, pada
tahun 1932, James Chadwick menemukan partikel netral, yang disebut neutron,
dari eksperimen bombardir partikel α pada berbagai unsur. Dengan demikian,
dapat disimpulkan bahwa dalam model awan elektron, awan elektron terdiri dari
elektron-elektron bermuatan negatif yang bergerak sangat cepat mengelilingi
inti atom yang tersusun dariproton yang bermuatan positif dan neutron yang tak
bermuatan.
Diadopsi dari :https://www.studiobelajar.com/teori-atom/










Tidak ada komentar